การแนะนำ
Pasireotide เป็น somatostatin แบบง่ายที่ได้รับการออกแบบทางวิศวกรรมซึ่งได้รับการพิจารณาที่สำคัญในพื้นที่ทางคลินิกสำหรับระบบการออกฤทธิ์ที่โดดเด่นและการใช้งานที่อาจเป็นประโยชน์ ในฐานะบุคคลจากตระกูล somatostatin ที่เรียบง่าย Pasireotide ทำงานโดยการจำกัดและการออกฤทธิ์ของตัวรับ somatostatin ในเนื้อเยื่อต่างๆ ทั่วร่างกาย ในรายการบล็อกนี้ เราจะตรวจสอบองค์ประกอบของกิจกรรมของปาสิรีโอไทด์โปรไฟล์การจำกัดตัวรับที่ชัดเจนเมื่อเปรียบเทียบกับสารอะนาล็อก somatostatin อื่นๆ และการขยายสาขาเพื่อการรักษาของคุณสมบัติทางเภสัชวิทยาที่ไม่ธรรมดา
 |
 |
กลไกการออกฤทธิ์ของ Pasireotide คืออะไร?
Pasireotide ก็เหมือนกับยาอะนาล็อก somatostatin อื่นๆ ที่จะจับและกระตุ้นการทำงานของตัวรับ somatostatin (SSTR) ตัวรับโซมาโตสแตตินที่ควบคู่กับโปรตีน G จะถูกติดตามในเนื้อเยื่อต่างๆ รวมถึงโครงร่างการดื้อยา อวัยวะต่อมใต้สมอง ตับอ่อน และล็อตระบบทางเดินอาหาร ชนิดย่อยทั้งห้าของตัวรับโซมาโตสเตติน ได้แก่ SSTR1, SSTR2, SSTR3, SSTR4 และ SSTR5 แต่ละชนิดมีการกระจายไปตามเนื้อเยื่อและหน้าที่ต่างๆ ในร่างกายไม่ซ้ำกัน
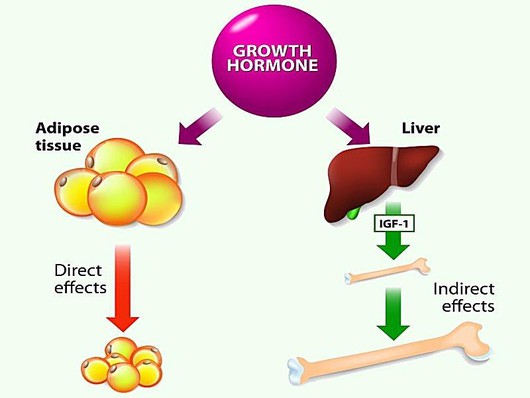
ปาสิรีโอไทด์เริ่มต้นเหตุการณ์การติดธงภายในเซลล์อย่างต่อเนื่องหลังจากจำกัดตัวเองไว้ที่ตัวรับโซมาโตสเตติน เหตุการณ์เหล่านี้ส่งผลให้เกิดการยับยั้งการปล่อยสารเคมีและการเปลี่ยนแปลงกระบวนการของเซลล์ในที่สุด วิธีหลักที่ pasireotide ป้องกันการหลั่งฮอร์โมนคือการยับยั้ง adenylyl cyclase ซึ่งจะช่วยลดระดับ cyclic AMP (cAMP) ในเซลล์ Cyclic AMP เป็นตัวส่งสารลำดับที่สองที่สำคัญที่เกี่ยวข้องกับการผสมและลักษณะของสารสังเคราะห์ที่เปลี่ยนแปลง คล้ายกับสารประกอบปรับปรุง (GH) ปัจจัยความก้าวหน้าคล้ายอินซูลิน-1 (IGF-1) และสารสังเคราะห์อะดรีโนคอร์ติโคโทรปิก ( แอคธ)
นอกจากผลกระทบต่อการหลั่งฮอร์โมนแล้ว ปาซิรีโอไทด์ยังแสดงให้เห็นว่าสามารถเปลี่ยนแปลงกระบวนการของเซลล์อื่นๆ เช่น การเพิ่มจำนวนเซลล์ การตายของเซลล์ และการสร้างเส้นเลือดใหม่ วิถีทางโปรตีนไคเนสที่กระตุ้นด้วยไมโทเจน (MAPK) และวิถีทางฟอสฟาทิดิลิโนซิทอล 3-ไคเนส (PI3K) เป็นสองวิถีทางที่ทำเครื่องหมายไว้ซึ่งมีแนวโน้มที่จะบรรลุผลกระทบเหล่านี้ Pasireotide มีศักยภาพในการออกฤทธิ์ต้านการแพร่กระจายและต้านเนื้องอกต่อการเจริญเติบโตของระบบประสาทและมะเร็งหลายชนิดโดยส่งผลต่อวิถีทางเหล่านี้
รูปแบบการจำกัดตัวรับอันเป็นเอกลักษณ์ของ Pasireotide ยังส่งผลต่อระบบกิจกรรมอีกด้วยปาสิรีโอไทด์สร้างความแตกต่างจากสารอะนาล็อกของโซมาโทสแตตินอื่นๆ เช่น Octreotide และ Lanreotide โดยมีความสัมพันธ์ในการจับสูงสำหรับซับไทป์ของตัวรับ somatostatin หลายตัว โดยเฉพาะ SSTR5 ในโรค Cushing ซึ่งเป็นความผิดปกติของระบบประสาทต่อมไร้ท่อ เนื้องอกในต่อมใต้สมองที่หลั่ง ACTH มีการแสดงออกของ SSTR5 ในระดับสูง ความมีชีวิตที่ได้รับการอัพเกรดนั้นเป็นเพราะโปรไฟล์การจำกัดตัวรับที่กว้าง
จำเป็นอย่างยิ่งที่ต้องจำไว้ว่าผลการรักษาของ Pasireotide อาจแตกต่างกันไปในแต่ละเนื้อเยื่อ ตัวอย่างเช่น Pasireotide ทำงานโดยทั่วไปเพื่อรักษาอะโครเมกาลีโดยการขัดขวางเซลล์ somatotroph ของอวัยวะต่อมใต้สมองไม่ให้ปล่อย GH และ IGF-1 ในทางกลับกัน กิจกรรมที่สำคัญของ Pasireotide ในการรักษาอาการเจ็บป่วยของ Cushing คือการยับยั้งการปล่อย ACTH จากเซลล์คอร์ติโคโทรฟ ซึ่งส่งผลให้การสร้างคอร์ติซอลต่อมหมวกไตลดลง
ความเข้าใจปาสิรีโอไทด์กลไกการออกฤทธิ์เป็นสิ่งสำคัญในการเพิ่มศักยภาพในการรักษาให้สูงสุดและคาดการณ์ผลข้างเคียงที่อาจเกิดขึ้น ด้วยการมุ่งเน้นไปที่ชนิดย่อยของตัวรับโซมาโตสแตตินที่หลากหลายและการเปลี่ยนแปลงวิถีการส่งสัญญาณที่หลากหลาย พาซิรีโอไทด์นำเสนอแนวทางใหม่ในการรักษาความผิดปกติของระบบประสาทต่อมไร้ท่อและสภาวะอื่นๆ ซึ่งตัวรับโซมาโตสตาตินมีบทบาทสำคัญในการเกิดโรคของโรค
โปรไฟล์การจำกัดตัวรับของ Pasireotide แตกต่างจากของอะนาล็อก somatostatin อื่น ๆ อย่างไร
Pasireotide โดดเด่นจากสารอะนาล็อก somatostatin อื่นๆ อย่างมากเนื่องจากมีโปรไฟล์จำกัดตัวรับที่ชัดเจน ตรงกันข้ามกับสารอะนาล็อกของโซมาโตสแตติน เช่น Octreotide และ Lanreotide ซึ่งจับกับ SSTR2 เป็นหลัก Pasireotide มีสัมพรรคภาพในการจับกับ SSTR1, SSTR2, SSTR3 และ SSTR5 มากกว่า
การเปลี่ยนแปลงหลักที่อะนาล็อกของโซมาโตสแตตินเกิดขึ้นสามารถรับผิดชอบต่อโปรไฟล์ที่จำกัดตัวรับเฉพาะที่แสดงอยู่ปาสิรีโอไทด์เป็นไซโคลเฮกซาเปปไทด์ที่มีคุณสมบัติจำกัดตัวรับเป็นพิเศษ เนื่องจากมีการกัดกร่อนของอะมิโนดั้งเดิมที่เรียกว่า (2-อะมิโนเอทิล)อะมิโนคาร์บอกซิลิกกัดกร่อน Pasireotide สามารถโต้ตอบกับชนิดย่อยของตัวรับ somatostatin ได้หลากหลาย โดยเฉพาะอย่างยิ่ง SSTR5 โดยมีการเลือกและความลำเอียงสูงเนื่องจากการดัดแปลงพื้นฐานนี้ ความเพียงพอที่เป็นประโยชน์ของ Pasireotide และผลที่ตามมาที่อาจเกิดขึ้นนั้นได้รับผลกระทบอย่างมากจากการจำกัดตัวรับในวงกว้าง เนื่องจากกำหนดเป้าหมายไปที่ชนิดย่อยของตัวรับ somatostatin หลายตัว pasireotide จึงสามารถยับยั้งการหลั่งฮอร์โมนและการเจริญเติบโตของเนื้องอกได้อย่างมีประสิทธิภาพมากกว่าสารอะนาล็อกของ somatostatin ที่คัดเลือกมามากกว่า
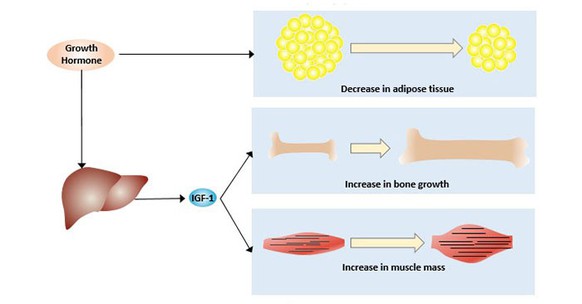
ตัวอย่างเช่น ในการรักษาอาการป่วยของ Cushing ความชื่นชอบ SSTR5 ของ Pasireotide เป็นสิ่งสำคัญอย่างยิ่ง การเจริญเติบโตของต่อมใต้สมองที่เปล่งแสงจาก ACTH ซึ่งเป็นตัวขับเคลื่อนสำคัญของการเจ็บป่วยของ Cushing แสดงถึงระดับ SSTR5 ที่สูงขึ้น ด้วยการมุ่งเน้นที่ SSTR5 โดยเฉพาะ Pasireotide สามารถยับยั้งการปล่อย ACTH และสร้างมาตรฐานระดับคอร์ติซอลในผู้ป่วยที่ป่วยด้วย Cushing ได้สำเร็จ ในทางกลับกัน Octreotide และ Lanreotide ประสบความสำเร็จในการรักษาโรคที่นอนเพียงจำกัด เนื่องจากพวกมันจับกับ SSTR2 เป็นหลัก
นอกจากนี้ ในการรักษาอะโครเมกาลี รูปแบบการจำกัดตัวรับที่กว้างของ Pasireotide อาจให้ประโยชน์มากกว่าอะนาล็อก somatostatin ที่เจาะจงมากกว่า เซลล์ Somatotroph ในอวัยวะต่อมใต้สมองแสดงชนิดย่อยของตัวรับ somatostatin ที่แตกต่างกัน รวมถึง SSTR2, SSTR3 และ SSTR5 ด้วยการมุ่งเน้นไปที่ชนิดย่อยของตัวรับที่แตกต่างกันเหล่านี้ Pasireotide สามารถยับยั้งการปล่อย GH และ IGF-1 ได้อย่างละเอียดถี่ถ้วนมากขึ้น กระตุ้นให้เกิดการควบคุมทางชีวเคมีและการช่วยเหลือผลข้างเคียงในผู้ป่วยที่มีอาการอะโครเมกาลี
อย่างไรก็ตาม โปรไฟล์ผลข้างเคียงที่ชัดเจนของ Pasireotide อาจได้รับอิทธิพลจากโปรไฟล์การจับตัวรับที่กว้างขวาง เมื่อเปรียบเทียบกับยาอะนาล็อก somatostatin อื่น Pasireotide มีความสัมพันธ์กับภาวะน้ำตาลในเลือดสูงซึ่งเป็นหนึ่งในผลข้างเคียงที่เห็นได้ชัดเจนที่สุด ความสัมพันธ์ที่สูงของ Pasireotide กับ SSTR5 ซึ่งแสดงออกในเซลล์เบต้าของตับอ่อนและเกี่ยวข้องกับการหลั่งอินซูลิน เชื่อว่าเป็นสาเหตุของสิ่งนี้ Pasireotide อาจทำให้เกิดหรือทำให้น้ำตาลในเลือดสูงเพิ่มขึ้นโดยการยับยั้งการหลั่งอินซูลิน จำเป็นต้องมีการตรวจสอบและจัดการระดับน้ำตาลในเลือดในระหว่างการรักษาอย่างระมัดระวัง
ลักษณะการจับตัวรับในวงกว้างของ Pasireotide และผลกระทบต่อระบบอวัยวะต่างๆ อาจเกี่ยวข้องกับผลข้างเคียงอื่นๆ ที่อาจเกิดขึ้น เช่น การรบกวนระบบทางเดินอาหาร โรคนิ่วในถุงน้ำดี และหัวใจเต้นช้า ด้วยวิธีนี้ การตัดสินใจระหว่าง Pasireotide และยาที่คล้ายกันของ somatostatin อื่นๆ ควรตั้งอยู่บนพื้นฐานการพิจารณาอย่างรอบคอบเกี่ยวกับสภาวะเฉพาะของผู้ป่วย วัตถุประสงค์ในการรักษา และอันตรายและข้อดีที่เป็นไปได้
สรุปแล้ว,ปาสิรีโอไทด์โดดเด่นจากสารอะนาล็อกโซมาโตสแตตินอื่นๆ เนื่องมาจากโปรไฟล์การจับรีเซพเตอร์ที่แตกต่างกัน ซึ่งมีลักษณะเฉพาะโดยสัมพรรคภาพสูงสำหรับซับไทป์ของรีเซพเตอร์โซมาโตสแตตินหลายชนิด โดยเฉพาะ SSTR5 โปรไฟล์การจำกัดตัวรับแบบกว้างนี้ช่วยเพิ่มความสามารถในการมีชีวิตในปัญหาเกี่ยวกับระบบประสาทต่อมไร้ท่อที่เฉพาะเจาะจง แต่ก็อาจเกี่ยวข้องกับโปรไฟล์ผลกระทบรองที่ไม่ผิดเพี้ยนเช่นกัน เมื่อเลือกตัวเลือกการรักษาที่ดีที่สุดสำหรับผู้ป่วยแต่ละรายและเพิ่มผลลัพธ์การรักษาให้สูงสุด จำเป็นอย่างยิ่งที่จะต้องเข้าใจความแตกต่างในการจับตัวรับของสารอะนาล็อกของ somatostatin
การใช้ Pasireotide ในการรักษาขึ้นอยู่กับกลไกการออกฤทธิ์อย่างไร?
Pasireotide ได้รับการตรวจสอบและอนุมัติเพื่อใช้ในการรักษาที่หลากหลาย โดยเฉพาะอย่างยิ่งในการจัดการความผิดปกติของระบบประสาทต่อมไร้ท่อ เนื่องจากมีกลไกการออกฤทธิ์เฉพาะตัวและโปรไฟล์การจับกับตัวรับ Pasireotide แสดงให้เห็นประสิทธิภาพในการรักษาสภาวะบางประการที่ยาทั่วไปมีข้อจำกัด โดยมุ่งเน้นไปที่ชนิดย่อยต่างๆ ของตัวรับ somatostatin และการเปลี่ยนแปลงการหลั่งของสารและกระบวนการของเซลล์
การรักษาโรค Cushing เป็นหนึ่งในการประยุกต์ใช้การรักษาที่มีชื่อเสียงที่สุดของ Pasireotide เนื่องจากเนื้องอกในต่อมใต้สมองที่หลั่ง ACTH โรค Cushing จึงเป็นความผิดปกติของระบบประสาทต่อมไร้ท่อที่หาได้ยากซึ่งมีลักษณะเฉพาะคือการหลั่งคอร์ติซอลมากเกินไป Pasireotide เป็นการตัดสินใจในการรักษาที่มีความหวังสำหรับภาวะนี้ เนื่องจากมีคำอธิบายพิเศษของ SSTR5 ในโรคต่อมใต้สมองที่ปล่อย ACTH Pasireotide ถูกแสดงไว้ในการทดลองทางคลินิกเพื่อปรับปรุงอาการทางคลินิก และลดระดับคอร์ติซอลอิสระในปัสสาวะอย่างมีนัยสำคัญในผู้ป่วยโรค Cushing ที่ไม่สามารถหรือไม่ได้รับการผ่าตัด

เป็นที่ทราบกันโดยทั่วไปว่าความสัมพันธ์ที่มีนัยสำคัญของ Pasireotide กับ SSTR5 ซึ่งส่งผลให้เกิดการยับยั้งการปล่อย ACTH จากเซลล์ corticotroph อย่างมีนัยสำคัญ เป็นกลไกหลักที่ทำให้ Pasireotide มีประสิทธิผลในโรค Cushing ด้วยการปรับระดับ ACTH และคอร์ติซอลให้เป็นปกติ ปาซิรีโอไทด์สามารถช่วยบรรเทาอาการหลายระบบของการติดเชื้อ Cushing ได้ เช่น ความผิดปกติทางเมตาบอลิซึม ภาวะแทรกซ้อนของหลอดเลือดหัวใจ และผลข้างเคียงทางระบบประสาทจิตเวช ในการรักษาอาการป่วยของ Cushing นั้น Pasireotide ได้แสดงให้เห็นถึงความเพียงพอและประวัติความเป็นอยู่ที่ดีก็ได้รับการแสดงเช่นกัน
การใช้ Pasireotide อย่างมากอีกอย่างหนึ่งคือการรักษา acromegaly Acromegaly เป็นภาวะที่น่าสนใจซึ่งเกิดจากการปล่อย GH ที่มากเกินไป ซึ่งมักเกิดจาก adenoma ต่อมใต้สมองที่ปล่อย GH การผลิต IGF ที่เพิ่มขึ้น-1 เกิดจากระดับ GH ที่เพิ่มขึ้น ส่งผลให้เกิดลักษณะเฉพาะของอะโครเมกาลี เช่น มือและเท้าที่พัฒนาแล้ว ใบหน้าที่หยาบขึ้น และปัญหาพื้นฐาน เช่น โรคเบาหวานและโรคหลอดเลือดหัวใจ
Pasireotide เป็นตัวเลือกการรักษาที่มีแนวโน้มสำหรับอะโครเมกาลี โดยเฉพาะอย่างยิ่งในผู้ป่วยที่ดื้อหรือแพ้ยาอะนาล็อก somatostatin ทั่วไป เช่น Octreotide และ Lanreotide เนื่องจากมีโปรไฟล์การจับตัวรับที่กว้างและความสัมพันธ์สูงสำหรับ SSTR2, SSTR3 และ SSTR5 ด้วยการมุ่งความสนใจไปที่ซับไทป์ของตัวรับโซมาโตสแตตินต่างๆ ให้เป็นศูนย์ Pasireotide จึงสามารถครอบคลุมระดับ GH และ IGF-1 ได้อย่างครอบคลุมมากขึ้น ซึ่งกระตุ้นให้เกิดการควบคุมทางชีวเคมีและผลกระทบทุติยภูมิในผู้ป่วยที่มีอาการอะโครเมกาลีลดลง
โดยคำนึงถึงองค์ประกอบของกิจกรรมปาสิรีโอไทด์ได้รับการตรวจสอบเพื่อใช้ในการบูรณะเพิ่มเติม แม้ว่าจะมีสัญญาณบ่งชี้อาการป่วยและอาการอะโครเมกาลีของ Cushing ก็ตาม Pasireotide ได้แสดงให้เห็นถึงคำมั่นสัญญาในการรักษาเนื้องอกที่หายาก เช่น เนื้องอกในระบบประสาทต่อมไร้ท่อ (NETs) ซึ่งมีต้นกำเนิดจากเซลล์ neuroendocrine ทั่วร่างกาย NET จำนวนมากมีตัวรับ Somatostatin โดยเฉพาะ SSTR2 และ SSTR5 ทำให้พวกมันกลายเป็นเป้าหมายในการรักษา
ลักษณะการจำกัดตัวรับแบบกวาดของ Pasireotide และฤทธิ์ต้านการแพร่ขยายของ Pasireotide ได้กระตุ้นให้เกิดการประเมินว่าเป็นการตัดสินใจในการรักษาสำหรับ NETs ทั้งสำหรับการควบคุมผลกระทบทุติยภูมิและข้อจำกัดในการปรับปรุงโรค ในการประเมินพรีคลินิก Pasireotide ได้แสดงให้เห็นผลในการต้านการแพร่กระจายและต้านเนื้องอกในแบบจำลอง NET ต่างๆ ซึ่งบ่งบอกถึงขีดจำกัดที่แท้จริงในฐานะการรักษาที่ได้รับมอบหมายสำหรับการพัฒนาเหล่านี้ ความมีชีวิตและความเป็นอยู่ที่ดีของ Pasireotide ในการรักษา NETs ไม่ว่าจะเพียงอย่างเดียวหรือเกี่ยวข้องกับวิธีการบูรณะอื่นๆ ล้วนขึ้นอยู่กับความคืบหน้าเบื้องต้นทางคลินิก
นอกจากนี้ ส่วนประกอบของกิจกรรมของ Pasireotide ยังชี้ให้เห็นถึงการใช้งานที่เป็นไปได้ในสถานการณ์ต่างๆ ซึ่งตัวรับ somatostatin มีบทบาทในการเกิดโรค ตัวอย่างเช่น โรคตับมีถุงน้ำหลายใบ ซึ่งเป็นภาวะทางพันธุกรรมที่ตับเกิดถุงน้ำหลายใบ ได้ถูกตรวจสอบว่าเป็นวิธีการรักษาที่เป็นไปได้ ตัวรับ Somatostatin โดยเฉพาะ SSTR2 และ SSTR5 จะถูกติดตามในตุ่มพองในตับ และจำได้ว่ามีส่วนในการพัฒนาแผลและการปล่อยของเหลวจากพวกมัน ด้วยการจับกับตัวรับเหล่านี้ ปาซิรีโอไทด์อาจลดปริมาตรของซีสต์โรคตับหลายใบและบรรเทาอาการได้
การใช้ประโยชน์เพื่อการบูรณะอื่นๆ ที่คาดหวังของปาสิรีโอไทด์เมื่อพิจารณาถึงระบบการทำงานของมัน ได้แก่ การบริหารภาวะน้ำตาลในเลือดต่ำเนื่องจากอินซูลินโนมา การเจริญเติบโตของระบบประสาทต่อมไร้ท่อในตับอ่อนที่ไม่ธรรมดาซึ่งหลั่งอินซูลินในปริมาณที่ไม่จำเป็น และการรักษาอะดีโนมาต่อมใต้สมองที่ไม่ทำงาน ซึ่งอาจสื่อสารตัวรับโซมาโตสเตติน และตอบการรักษาแบบง่ายของโซมาโทสแตติน
เมื่อพิจารณาทุกอย่างแล้ว การใช้ Pasireotide เพื่อการบูรณะนั้นได้รับแรงหนุนจากองค์ประกอบที่น่าสนใจของกิจกรรมและโปรไฟล์การจำกัดตัวรับที่กว้าง Pasireotide ได้รับการพิสูจน์แล้วว่ามีประสิทธิภาพในการรักษาโรค Cushing, Acromegaly และความผิดปกติของระบบประสาทต่อมไร้ท่ออื่น ๆ โดยการมุ่งเน้นไปที่ชนิดย่อยที่หลากหลายของตัวรับ somatostatin และการเปลี่ยนแปลงการหลั่งฮอร์โมนและกระบวนการของเซลล์ ขอบเขตที่เพิ่มขึ้นของการประยุกต์ใช้ในการรักษาของ Pasireotide นั้นเน้นไปที่การใช้ที่มีศักยภาพใน NETs โรคตับที่มีถุงน้ำหลายใบ และเงื่อนไขอื่นๆ ที่ตัวรับ somatostatin มีส่วนเกี่ยวข้องในการเกิดโรค Pasireotide อาจกลายเป็นทางเลือกในการรักษาที่มีประโยชน์สำหรับสภาวะทางการแพทย์ที่หลากหลาย เนื่องจากความซับซ้อนของการส่งสัญญาณของตัวรับ somatostatin และบทบาทของมันในโรคต่างๆ เป็นที่เข้าใจได้ดีขึ้น
อ้างอิง:
1. Colao, A., Petersenn, S., Newell-Price, J., Findling, JW, Gu, F., Maldonado, M., ... & Boscaro, M. (2012) การศึกษา 12-ระยะที่ 3 ของเดือนเกี่ยวกับปาสิรีโอไทด์ในโรคคุชชิง วารสารการแพทย์นิวอิงแลนด์, 366(10), 914-924
2. ลาครัวซ์, เอ., กู, เอฟ., กัลลาร์โด, ดับเบิลยู., ปิโวเนลโล, อาร์., ยู, วาย., วิทเทค, พี., ... & บอสกาโร, เอ็ม. (2018) ประสิทธิภาพและความปลอดภัยของปาสิรีโอไทด์เดือนละครั้งในโรคคุชชิง: การทดลองทางคลินิก 12 เดือน มีดหมอเบาหวานและวิทยาต่อมไร้ท่อ, 6(1), 17-26
3. Gadelha, MR, Bronstein, MD, Brue, T., Coculescu, M., Fleseriu, M., Guitelman, M., ... & กลุ่มศึกษา Pasireotide C2305 (2014) Pasireotide เทียบกับการรักษาด้วย octreotide หรือ lanreotide อย่างต่อเนื่องในผู้ป่วยที่มี acromegaly ที่มีการควบคุมไม่เพียงพอ (PAOLA): การทดลองแบบสุ่มระยะที่ 3 มีดหมอเบาหวานและวิทยาต่อมไร้ท่อ, 2(11), 875-884
4. Cives, M., Kunz, PL, Morse, B., Coppola, D., Schell, MJ, Campos, T., ... & Strosberg, JR (2015) การทดลองทางคลินิกระยะที่ 2 ของการปลดปล่อย pasireotide ที่ออกฤทธิ์นานในผู้ป่วยที่มีเนื้องอกในระบบประสาทต่อมไร้ท่อระยะลุกลาม มะเร็งที่เกี่ยวข้องกับต่อมไร้ท่อ, 22(1), 1-9
5. Gessl, A., Blum, S., Schmid-Braz, AT, Riss, P., Selberherr, A., Marosi, C., ... & Haug, AR (2020) ประสิทธิภาพและความปลอดภัยของ pasireotide ในการควบคุมอาการในผู้ป่วยที่มีเนื้องอก neuroendocrine ระยะลุกลาม รายงานทางวิทยาศาสตร์, 10(1), 1-8
6. Van der Velden, S., Beljaars, L., Harms, A., Wedel, J., Bijvelds, M., Lenders, M., ... & Meijer, C. (2020) การให้ Pasireotide ใต้ผิวหนังจะถูกดูดซึมได้อย่างรวดเร็วและแสดงระยะเวลาพักเฉลี่ยที่สั้นในผู้ป่วยที่เป็นโรคตับ polycystic ที่มีอาการ วารสารยุโรปด้านการเผาผลาญยาและเภสัชจลนศาสตร์, 45(5), 633-641
7. ปีเตอร์เซนน์, เอส., ซัลกาโด, LR, สโชโพห์ล, เจ., ปอร์โตคาร์เรโร-ออร์ติซ, แอล., อาร์นัลดี, จี., ลาครัวซ์, เอ., ... & บิลเลอร์, บีเอ็ม (2017) การรักษาโรคคุชชิงในระยะยาวด้วยปาซิรีโอไทด์: 5- ปีเป็นผลจากการศึกษาแบบ open-label extension ของการทดลองระยะที่ 3 ต่อมไร้ท่อ, 57(1), 156-165
8. Bruns, C., Lewis, I., Briner, U., Meno-Tetang, G., & Weckbecker, G. (2002) SOM230: somatostatin peptidomimetic ใหม่ที่มีการจับตัวรับ somatotropin release inhibitoring factor (SRIF) ในวงกว้างและโปรไฟล์ antisecretory ที่เป็นเอกลักษณ์ วารสารต่อมไร้ท่อแห่งยุโรป, 146(5), 707-716
9. ชมิด, เอชเอ (2008) Pasireotide (SOM230): การพัฒนา กลไกการออกฤทธิ์ และการประยุกต์ใช้ที่เป็นไปได้ วิทยาต่อมไร้ท่อระดับโมเลกุลและเซลล์ 286(1-2), 69-74
10. D. Cuevas-Ramos, & Fleseriu, M. (2014). โซมาโตสตาติน

